2023-02-03
化学沉淀法
化学沉淀法
一、工艺简介
向废水中投加某些化学物质,使它和废水中欲去除的污染物发生直接的化学反应,生成难溶于水的沉淀物而使污染物分离除去的一种废水处理方法。但由于化学法普遍要加入大量的化学药剂,并成为沉淀物的形式沉淀出来。这就决定了化学法处理后会存在大量的二次污染,如大量废渣的产生,而这些废渣的处理目前尚无较好的处理处置方法,所以对其在工程上的应用和以后的可持续发展都存在巨大的负面作用。
化学沉淀法经常用于处理含有汞、铅、铜、锌、六价铬、硫、氰、氟、砷等有毒化合物的废水。利用向废水中投加氢氧化物、硫化物、碳酸盐、卤化物等生成金属盐沉淀可以去除废水中的金属离子,向废水中投加钡盐可用于处理含六价铬的工业废水生成铬酸盐沉淀,向废水中投加石灰生成氟化钙沉淀可以去除水中的氟化物。根据使用的沉淀剂不同,常见的化学沉淀法有氢氧化物沉淀法、硫化物沉淀法、碳酸盐沉淀法、钡盐沉淀法、卤化物沉淀法等。
化学沉淀法可用于去除废水中氟、磷、铅、砷。
二、工艺原理
(一)化学沉淀法除氟原理:
化学沉淀除氟工艺采用石灰反应法。根据氟的化学性质,氟可与多种金属离子形成稳定的化合物,作为环境治理,为取得投入少,见效较好的结果,选择钙离子作为沉淀剂较为合理,形成难溶的氟化钙(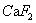 ),以固液分离手段从废水中去除。其基本化学反应式如下:
),以固液分离手段从废水中去除。其基本化学反应式如下:
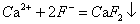 (1 )
(1 )
 是一种相当稳定的化合物,其溶度积达到
是一种相当稳定的化合物,其溶度积达到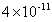 ,因此,用钙离子作为沉淀剂处理后的水溶液中,理论上的氟含量可达到
,因此,用钙离子作为沉淀剂处理后的水溶液中,理论上的氟含量可达到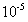 ,可以满足环保的要求。但在25℃时,
,可以满足环保的要求。但在25℃时,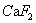 在水中的饱和溶解度为16.5mg/L,其中
在水中的饱和溶解度为16.5mg/L,其中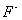 占8.03mg/L,所以,在工程中比较实际的方法是,仍以
占8.03mg/L,所以,在工程中比较实际的方法是,仍以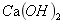 作为中和剂,应用同离子效应理论,控制处理后出水中
作为中和剂,应用同离子效应理论,控制处理后出水中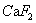 的饱和溶解度。
的饱和溶解度。
同离子效应理论认为,在难溶电解质的饱和溶液中,加入含有同离子的另一种电解质时,原有的电解质溶解度降低。含氟废水中加入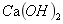 ,可以生成
,可以生成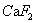 。随着反应的进行,
。随着反应的进行,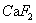 的浓度不断升高。当
的浓度不断升高。当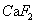 的浓度超过了饱和溶解度时,就会有固体
的浓度超过了饱和溶解度时,就会有固体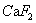 析出。溶液能否有固体析出,是根据溶度积规则判断。就
析出。溶液能否有固体析出,是根据溶度积规则判断。就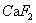 而言,它的溶度积规则形式为:
而言,它的溶度积规则形式为:
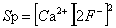 (2)
(2)
式中: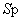 ————溶度积常数。
————溶度积常数。
 ————溶液中
————溶液中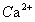 浓度,摩尔浓度(mol/L)。
浓度,摩尔浓度(mol/L)。
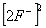 ————溶液中
————溶液中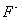 浓度,摩尔浓度(mol/L)。
浓度,摩尔浓度(mol/L)。
由于分子式是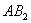 型,所以为2
型,所以为2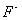 。
。
溶度积常数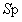 只是随温度变化而变化。当温度一定时溶度积常数
只是随温度变化而变化。当温度一定时溶度积常数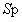 则为一个定值。从(2)式中可以看出,提高溶液中
则为一个定值。从(2)式中可以看出,提高溶液中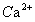 的浓度,
的浓度,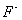 的浓度就会相应降低,从而使
的浓度就会相应降低,从而使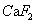 的溶解度下降。
的溶解度下降。
氯化钙溶解性很好,能有效提高溶液中钙离子的浓度,当与消石灰并用时产生同离子效应,使方程(1)平衡向右移动而有效降低氟离子的浓度,强化了沉淀效果,而且氯化钙是一种中性盐,投加后不会对PH值产生影响。
(二)化学沉淀法除磷原理:
废水除磷一般有传统生物法和化学沉淀法。
传统的生物处理法工艺操作简单 ,但磷去除效率较低 ,难以满足出水要求;化学沉淀法除磷工艺虽除磷效率相对较高 ,但消耗化学药剂并产生大量的化学污泥 ,处理成本相对昂贵。
生物法除磷原理:
生物法除磷的原理是某些细菌交替地处于厌氧与好氧条件下 ,在厌氧时 ,细菌吸收低分子的有机物并以聚β-2羟基丁酸( PHB)等形式在体内储存起来 ,同时将细胞原生质中聚合磷酸盐以正磷酸盐的方式释放出来 ,此时污水中磷的含量升高 ,BOD 的含量降低。然后在好氧条件下 ,细菌将吸收的有机物(PHB)氧化分解 ,并提供能源 ,同时从污水中吸收大量的磷 ,以聚磷酸盐的形式储存起来 ,其吸收的量大于其释放的量 ,这时污水中的磷含量大大降低 ,通过把剩余污泥排出系统 ,同时将细菌摄入的磷排走从而达到除磷的目的。
化学沉淀法除磷原理:
化学除磷的基本原理主要分为:沉淀反应、凝聚作用、絮凝作用、固液分离。沉淀反应和凝聚过程在一个混合单元内进行,目的是使沉淀剂在污水中快速有效地混合。凝聚过程中,沉淀所形成的胶体和污水中原已存在的胶体凝聚为直径在10~15μm范围内的主粒子。絮凝过程中主粒子相互结合在一起形成更大的粒子絮体,该过程的意义在于增加沉淀物颗粒的大小,使得这些颗粒能够通过典型的沉淀或气浮加以分离,固液分离可单独进行,也可与初沉污泥和二沉污泥的排放相结合。可用于化学除磷的金属盐有三种:钙盐、铁盐和铝盐,最常用的是石灰、硫酸铝、铝酸钠、三氧化铁、硫酸铁、硫酸亚铁和氯化亚铁。一般认为磷酸盐沉淀是配位基参与竞争的电性中和沉淀,即通过与铝离子、铁离子或钙离子的化学沉淀作用加以去除。磷酸盐沉淀常有伴生反应,产物具有絮凝作用。在一定条件下,磷酸盐沉淀可能是化学络合起主要作用,而不是以电性中和为主。J.P.Boisseret[12]通过对硫酸铝和聚硫酸硅铝(PASS)的研究表明,磷的吸附和去除主要是一种特殊作用力下的络合反应的结果。Elisabet在其研究中指出,特别是正磷酸盐的去除过程中,氢氧化铝的吸附起很重要的作用,而不是典型的化学沉淀起主要作用。
(三)化学沉淀法除铅原理:
铅常被用作原料应用于蓄电池、电镀、颜料、橡胶、农药、燃料等制造业。铅板制作工艺中排放的酸性废水(pH3=铅浓度最高,电镀废液产生的废水铅浓度也很高。 铅是自然界分布很广的元素, 也是工业中常使用的元素之一。铅和可溶性铅盐都有毒性, 含铅废水对人体健康和动植物生长都有严重危害。如每日摄取铅量超过0.3-1.0 mg, 就可在人体内积累, 引起贫血、神经炎等。随着工业技术的迅速发展, 工业废水中的重金属铅作为一类污染物, 国家排放标准中明确规定含铅废水的排放标准为铅总含1 mg/ L。
一、含铅废水的来源
含铅废水来自各种电池车间、选矿厂、石油化工厂等。电池工业是含铅废水的最主要来源, 据报道, 每生产1 个电池就造成铅损失4.54-6810mg, 其次是石油工业生产汽油添加剂。
尽管铅不如铜、镉那样常见, 但它却是废水中的普通组分。尤其是电池厂在生产过程中产生大量含铅废水, 废水中铅含量超出国家标准百倍, 对地下水源构成很大威胁, 如果不进行处理而任意排放, 必然给环境与社会带来极大的危害。
二、含铅废水处理工艺
目前含铅废水的处理工艺,应用较多、较成熟可靠的技术有:离子交换法、沉淀法、吸附法、电解法以及以上工艺的组合。
1. 离子交换法 离子交换法的原理是利用离子交换剂分离废水中有害物质的方法,常用的离子交换剂有离子交换树脂、沸石等。离子交换是靠交换剂自身所带的能自由移动的离子与被处理的溶液中的离子通过离子交换来实现的。推动离子交换的动力是离子间浓度差和交换剂上的功能基对离子的亲和能力。
在对炸药厂废水的处理研究中,使用强酸性阳离子交换树脂、在pH值5.0—5.2时,用磷酸树脂对排放水进行离子交换处理,铅含量可降到O.20一O.53mg/L;在对离子交换工艺及相应工艺条件运行及考察,含铅量10m∥L的废水经离子交换处理,排出水含铅量为0.14一O.18mg/L,达到国家排放水质量标准。利用由氯甲基化交联的聚苯乙烯氧化制得的带羧基的弱酸树脂强酸性阳离子交换树脂,在pH=2.5、流速为15夥小时,可以处理700倍树脂体积的废液流,排放量可以达到0.01毫影升以下。
离子交换法除铅工艺的特点是:a.除铅彻底,工业含铅废水可实现达标排放。b.对环境污染危害小,污泥少。c.离子交换树脂的使用寿命长达5年以上,可经再生反复使用。d.离子交换装置占地面积小。
2. 吸附法 吸附法也是一种常用的含铅废水处理工艺,根据它的作用机理的不同也可以分为物理吸附法和生物吸附法。
1) 物理吸附法 物理吸附法是利用吸附剂特殊的物理化学性质,如较高的表面活性、较大的比表面积、特殊的微孔结构等。常用的吸附剂有改性膨润土、粉煤灰、沸石、陶土、活性炭等。这种处理工艺具有除铅效率高、成本适中、不造成二次污染的特点,因此具有良好的使用前景,特别是对一些吸附剂的改性之后处理效果更加可观。
2) 生物吸附法 微生物对重金属具有很强的亲和吸附性能,通过物理化学作用将重金属吸附在胞外聚合物的结合点上,从而从水中去除,活的和死的微生物对重金属离子都有较强的吸附能力。这些微生物主要有藻类、真菌、细菌等。该法以其原材料来源丰富、成本低、吸附速度快、吸附量大、选择性好、无毒、无害、无二次污染等特点正受到越来越多的重视。
3. 电解法
电解法的原理是重金属离子在阴极表面得到电子而被还原为金属。电解法处理废水一般无需加入很多化学药品,处理简单、占地面积小、管理方便、污泥量小,所以被称为清洁处理法。这种方法可直接得到纯金属,可以回收使用重金属。三维电极电解法的提出是电解法的革新,使得含铅废水通过点解法的深度进化成为可能。三维电极电解法通过增大电极表面积实现低电流密度下电解,减小了浓差极化,从而提高了电流效率。目前使用三维电极电解处理废水中的Cu“已经取得了较好的效果,并已应用于实践中。R-C•Wjdener等人使用网状玻璃炭电极对酸性含铅废水进行了研究,在一O.8 V(vs.SCE)的电位下,使用O.5moL/L硼酸作缓冲溶液,得出最佳条件是阴极孔隙率80 ppi,流速240L/h。可使初始浓度为50mg/L的含铅废水降至0.1 mg/L,电流效率还可达到14%。实现了含铅废水的深度净化。
(四)化学沉淀法除砷原理:
水体中的砷如何去除:目前,国内外处理污水处理中含砷废水的方法主要有沉淀法、离子交换法、生物法、膜法、电凝聚法、吸附法等。这些方法均有其自身的特点,如:沉淀法除砷技术较为完善,应用较为广泛,但它处理后会产生大量废渣,造成二次污染,而且除砷效率低,难以满足饮用水水质要求;离子交换法适用于处理量不大、组成单一、回收价值高的废水,但其处理工艺复杂、成本高,难以实现工业化生产;生物法中微生物对周边环境的要求很严格,因砷具有毒性,用此法处理水中的砷目前尚处在起步阶段;膜分离法处理成本较高,不宜大规模应用;电凝聚法操作技术条件要求比较高;吸附法是利用吸附剂提供的大比表面积,通过砷污染物与吸附剂间较强的亲和力达到净化除砷的目的。吸附法由于简单易行、去除效果好、能回收废水中的砷、对环境不产生或很少产生二次污染,且吸附材料来源广泛、价格低廉、可重复使用等优势而备受人们关注。
石灰法除砷原理:
一般适用于含砷较高的酸性废水。投加石灰乳,使其与砷酸根或亚砷酸跟离子发生反应,生成难溶解的砷酸钙或亚砷酸钙沉淀。
化学原理:
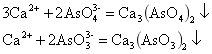
废水投加石灰乳混合沉淀,当石灰乳投加适当,反应进行的完全时,出水水质可到达污水综合排放标准(GB8978-88).
此方法的缺点是反应较慢,而且生成的砷酸钙与亚砷酸钙在水中的溶解性较大。
石灰-铁盐法除砷原理:
一般用于含砷量较低的,PH值接近中性或者弱碱性的废水处理,利用砷酸盐或亚砷酸盐能与铁、铝等金属离子形成稳定的络合物,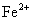 在鼓入空气的条件下转变成
在鼓入空气的条件下转变成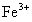 ,同时
,同时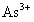 转变成毒性较小的
转变成毒性较小的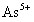 ,从而生成溶度积非常小(
,从而生成溶度积非常小(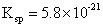 )的
)的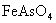 沉淀。另外
沉淀。另外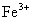 的水解产物
的水解产物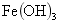 对一些难降解的细小的
对一些难降解的细小的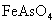 和
和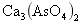 颗粒有吸附、凝聚、网捕的作用。
颗粒有吸附、凝聚、网捕的作用。
硫酸亚铁铁离子除砷法是利用铁离子或其化合物对砷离子进行吸附共沉来达到除砷的目的。这种方法主硫酸亚铁除砷要针对砷的水体污染。这种方法除砷,对水体中的酸碱性要求比较高,一般是在5.5-8.5这个范围内,一般是对含砷污水添加硫酸亚铁等铁盐混凝剂进行酸碱调节(硫酸亚铁处理碱性废水),同时增加污水中铁的含量。水中的铁离子含量保持在或者高于1.5mg/l。所投加的铁离子与污水中的砷离子的比例不得少于20:1,就可以使其去除率达到80%-95%。
废水中砷主要以正亚砷酸和偏亚砷酸及它们的盐类的形式存在,废水中有下列电离平衡:
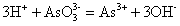
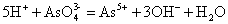
在废水中加入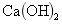 、
、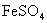 时,铁和废水中
时,铁和废水中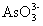 、
、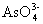 形成稳定的络合物,并被铁的氢氧化物吸附共沉而达到除砷的目的:
形成稳定的络合物,并被铁的氢氧化物吸附共沉而达到除砷的目的:

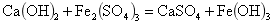
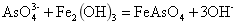
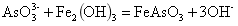
其中,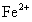 有很强的还原性,在溶液中很容易被氧化成
有很强的还原性,在溶液中很容易被氧化成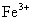 。
。
硫化物法除砷原理:
在酸性条件下,砷以阳离子形式存在,当加入硫化剂时,生成难溶的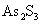 沉淀。硫化法净化效果较好,可使废水中含砷量将至0.05mg/L一下。废水PH值与转化法除砷的关系由废水砷化合物的性质决定的,砷酸和亚砷酸均为两性化合物,在水中既能按酸式电离,也能按碱式电离。酸性条件下,碱式电离将向生成砷离子方向移动。
沉淀。硫化法净化效果较好,可使废水中含砷量将至0.05mg/L一下。废水PH值与转化法除砷的关系由废水砷化合物的性质决定的,砷酸和亚砷酸均为两性化合物,在水中既能按酸式电离,也能按碱式电离。酸性条件下,碱式电离将向生成砷离子方向移动。
主要化学反应式如下:
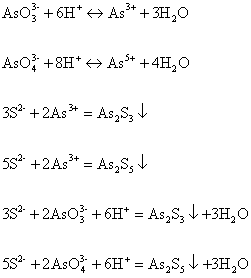
但硫化物沉淀需要在酸性条件下进行,否则沉淀物难以过滤,上清液中存在过剩的硫离子,在排放之前,需要进一步的处理。由于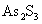 沉淀物只有在酸性环境中才能稳定,当PH值>1时,
沉淀物只有在酸性环境中才能稳定,当PH值>1时,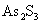 将会重新溶解到废酸溶液中,所以处理过程中,硫化物的加入量控制非常关键,硫化物投入量不足时,不能充分去除砷氧化物;投入量过多,又会过多消耗废酸溶液中的
将会重新溶解到废酸溶液中,所以处理过程中,硫化物的加入量控制非常关键,硫化物投入量不足时,不能充分去除砷氧化物;投入量过多,又会过多消耗废酸溶液中的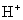 离子,使酸度过低,甚至呈碱性,造成
离子,使酸度过低,甚至呈碱性,造成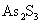 的重新溶解。这两种情况都会使除砷效率严重下降。
的重新溶解。这两种情况都会使除砷效率严重下降。
一、工艺简介
向废水中投加某些化学物质,使它和废水中欲去除的污染物发生直接的化学反应,生成难溶于水的沉淀物而使污染物分离除去的一种废水处理方法。但由于化学法普遍要加入大量的化学药剂,并成为沉淀物的形式沉淀出来。这就决定了化学法处理后会存在大量的二次污染,如大量废渣的产生,而这些废渣的处理目前尚无较好的处理处置方法,所以对其在工程上的应用和以后的可持续发展都存在巨大的负面作用。
化学沉淀法经常用于处理含有汞、铅、铜、锌、六价铬、硫、氰、氟、砷等有毒化合物的废水。利用向废水中投加氢氧化物、硫化物、碳酸盐、卤化物等生成金属盐沉淀可以去除废水中的金属离子,向废水中投加钡盐可用于处理含六价铬的工业废水生成铬酸盐沉淀,向废水中投加石灰生成氟化钙沉淀可以去除水中的氟化物。根据使用的沉淀剂不同,常见的化学沉淀法有氢氧化物沉淀法、硫化物沉淀法、碳酸盐沉淀法、钡盐沉淀法、卤化物沉淀法等。
化学沉淀法可用于去除废水中氟、磷、铅、砷。
二、工艺原理
(一)化学沉淀法除氟原理:
化学沉淀除氟工艺采用石灰反应法。根据氟的化学性质,氟可与多种金属离子形成稳定的化合物,作为环境治理,为取得投入少,见效较好的结果,选择钙离子作为沉淀剂较为合理,形成难溶的氟化钙(
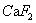 ),以固液分离手段从废水中去除。其基本化学反应式如下:
),以固液分离手段从废水中去除。其基本化学反应式如下: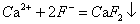 (1 )
(1 ) 是一种相当稳定的化合物,其溶度积达到
是一种相当稳定的化合物,其溶度积达到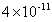 ,因此,用钙离子作为沉淀剂处理后的水溶液中,理论上的氟含量可达到
,因此,用钙离子作为沉淀剂处理后的水溶液中,理论上的氟含量可达到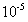 ,可以满足环保的要求。但在25℃时,
,可以满足环保的要求。但在25℃时,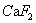 在水中的饱和溶解度为16.5mg/L,其中
在水中的饱和溶解度为16.5mg/L,其中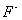 占8.03mg/L,所以,在工程中比较实际的方法是,仍以
占8.03mg/L,所以,在工程中比较实际的方法是,仍以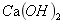 作为中和剂,应用同离子效应理论,控制处理后出水中
作为中和剂,应用同离子效应理论,控制处理后出水中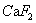 的饱和溶解度。
的饱和溶解度。同离子效应理论认为,在难溶电解质的饱和溶液中,加入含有同离子的另一种电解质时,原有的电解质溶解度降低。含氟废水中加入
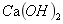 ,可以生成
,可以生成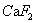 。随着反应的进行,
。随着反应的进行,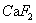 的浓度不断升高。当
的浓度不断升高。当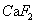 的浓度超过了饱和溶解度时,就会有固体
的浓度超过了饱和溶解度时,就会有固体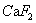 析出。溶液能否有固体析出,是根据溶度积规则判断。就
析出。溶液能否有固体析出,是根据溶度积规则判断。就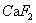 而言,它的溶度积规则形式为:
而言,它的溶度积规则形式为: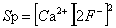 (2)
(2)式中:
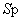 ————溶度积常数。
————溶度积常数。 ————溶液中
————溶液中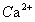 浓度,摩尔浓度(mol/L)。
浓度,摩尔浓度(mol/L)。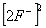 ————溶液中
————溶液中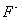 浓度,摩尔浓度(mol/L)。
浓度,摩尔浓度(mol/L)。由于分子式是
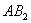 型,所以为2
型,所以为2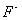 。
。溶度积常数
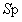 只是随温度变化而变化。当温度一定时溶度积常数
只是随温度变化而变化。当温度一定时溶度积常数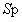 则为一个定值。从(2)式中可以看出,提高溶液中
则为一个定值。从(2)式中可以看出,提高溶液中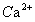 的浓度,
的浓度,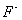 的浓度就会相应降低,从而使
的浓度就会相应降低,从而使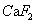 的溶解度下降。
的溶解度下降。氯化钙溶解性很好,能有效提高溶液中钙离子的浓度,当与消石灰并用时产生同离子效应,使方程(1)平衡向右移动而有效降低氟离子的浓度,强化了沉淀效果,而且氯化钙是一种中性盐,投加后不会对PH值产生影响。
(二)化学沉淀法除磷原理:
废水除磷一般有传统生物法和化学沉淀法。
传统的生物处理法工艺操作简单 ,但磷去除效率较低 ,难以满足出水要求;化学沉淀法除磷工艺虽除磷效率相对较高 ,但消耗化学药剂并产生大量的化学污泥 ,处理成本相对昂贵。
生物法除磷原理:
生物法除磷的原理是某些细菌交替地处于厌氧与好氧条件下 ,在厌氧时 ,细菌吸收低分子的有机物并以聚β-2羟基丁酸( PHB)等形式在体内储存起来 ,同时将细胞原生质中聚合磷酸盐以正磷酸盐的方式释放出来 ,此时污水中磷的含量升高 ,BOD 的含量降低。然后在好氧条件下 ,细菌将吸收的有机物(PHB)氧化分解 ,并提供能源 ,同时从污水中吸收大量的磷 ,以聚磷酸盐的形式储存起来 ,其吸收的量大于其释放的量 ,这时污水中的磷含量大大降低 ,通过把剩余污泥排出系统 ,同时将细菌摄入的磷排走从而达到除磷的目的。
化学沉淀法除磷原理:
化学除磷的基本原理主要分为:沉淀反应、凝聚作用、絮凝作用、固液分离。沉淀反应和凝聚过程在一个混合单元内进行,目的是使沉淀剂在污水中快速有效地混合。凝聚过程中,沉淀所形成的胶体和污水中原已存在的胶体凝聚为直径在10~15μm范围内的主粒子。絮凝过程中主粒子相互结合在一起形成更大的粒子絮体,该过程的意义在于增加沉淀物颗粒的大小,使得这些颗粒能够通过典型的沉淀或气浮加以分离,固液分离可单独进行,也可与初沉污泥和二沉污泥的排放相结合。可用于化学除磷的金属盐有三种:钙盐、铁盐和铝盐,最常用的是石灰、硫酸铝、铝酸钠、三氧化铁、硫酸铁、硫酸亚铁和氯化亚铁。一般认为磷酸盐沉淀是配位基参与竞争的电性中和沉淀,即通过与铝离子、铁离子或钙离子的化学沉淀作用加以去除。磷酸盐沉淀常有伴生反应,产物具有絮凝作用。在一定条件下,磷酸盐沉淀可能是化学络合起主要作用,而不是以电性中和为主。J.P.Boisseret[12]通过对硫酸铝和聚硫酸硅铝(PASS)的研究表明,磷的吸附和去除主要是一种特殊作用力下的络合反应的结果。Elisabet在其研究中指出,特别是正磷酸盐的去除过程中,氢氧化铝的吸附起很重要的作用,而不是典型的化学沉淀起主要作用。
(三)化学沉淀法除铅原理:
铅常被用作原料应用于蓄电池、电镀、颜料、橡胶、农药、燃料等制造业。铅板制作工艺中排放的酸性废水(pH3=铅浓度最高,电镀废液产生的废水铅浓度也很高。 铅是自然界分布很广的元素, 也是工业中常使用的元素之一。铅和可溶性铅盐都有毒性, 含铅废水对人体健康和动植物生长都有严重危害。如每日摄取铅量超过0.3-1.0 mg, 就可在人体内积累, 引起贫血、神经炎等。随着工业技术的迅速发展, 工业废水中的重金属铅作为一类污染物, 国家排放标准中明确规定含铅废水的排放标准为铅总含1 mg/ L。
一、含铅废水的来源
含铅废水来自各种电池车间、选矿厂、石油化工厂等。电池工业是含铅废水的最主要来源, 据报道, 每生产1 个电池就造成铅损失4.54-6810mg, 其次是石油工业生产汽油添加剂。
尽管铅不如铜、镉那样常见, 但它却是废水中的普通组分。尤其是电池厂在生产过程中产生大量含铅废水, 废水中铅含量超出国家标准百倍, 对地下水源构成很大威胁, 如果不进行处理而任意排放, 必然给环境与社会带来极大的危害。
二、含铅废水处理工艺
目前含铅废水的处理工艺,应用较多、较成熟可靠的技术有:离子交换法、沉淀法、吸附法、电解法以及以上工艺的组合。
1. 离子交换法 离子交换法的原理是利用离子交换剂分离废水中有害物质的方法,常用的离子交换剂有离子交换树脂、沸石等。离子交换是靠交换剂自身所带的能自由移动的离子与被处理的溶液中的离子通过离子交换来实现的。推动离子交换的动力是离子间浓度差和交换剂上的功能基对离子的亲和能力。
在对炸药厂废水的处理研究中,使用强酸性阳离子交换树脂、在pH值5.0—5.2时,用磷酸树脂对排放水进行离子交换处理,铅含量可降到O.20一O.53mg/L;在对离子交换工艺及相应工艺条件运行及考察,含铅量10m∥L的废水经离子交换处理,排出水含铅量为0.14一O.18mg/L,达到国家排放水质量标准。利用由氯甲基化交联的聚苯乙烯氧化制得的带羧基的弱酸树脂强酸性阳离子交换树脂,在pH=2.5、流速为15夥小时,可以处理700倍树脂体积的废液流,排放量可以达到0.01毫影升以下。
离子交换法除铅工艺的特点是:a.除铅彻底,工业含铅废水可实现达标排放。b.对环境污染危害小,污泥少。c.离子交换树脂的使用寿命长达5年以上,可经再生反复使用。d.离子交换装置占地面积小。
2. 吸附法 吸附法也是一种常用的含铅废水处理工艺,根据它的作用机理的不同也可以分为物理吸附法和生物吸附法。
1) 物理吸附法 物理吸附法是利用吸附剂特殊的物理化学性质,如较高的表面活性、较大的比表面积、特殊的微孔结构等。常用的吸附剂有改性膨润土、粉煤灰、沸石、陶土、活性炭等。这种处理工艺具有除铅效率高、成本适中、不造成二次污染的特点,因此具有良好的使用前景,特别是对一些吸附剂的改性之后处理效果更加可观。
2) 生物吸附法 微生物对重金属具有很强的亲和吸附性能,通过物理化学作用将重金属吸附在胞外聚合物的结合点上,从而从水中去除,活的和死的微生物对重金属离子都有较强的吸附能力。这些微生物主要有藻类、真菌、细菌等。该法以其原材料来源丰富、成本低、吸附速度快、吸附量大、选择性好、无毒、无害、无二次污染等特点正受到越来越多的重视。
3. 电解法
电解法的原理是重金属离子在阴极表面得到电子而被还原为金属。电解法处理废水一般无需加入很多化学药品,处理简单、占地面积小、管理方便、污泥量小,所以被称为清洁处理法。这种方法可直接得到纯金属,可以回收使用重金属。三维电极电解法的提出是电解法的革新,使得含铅废水通过点解法的深度进化成为可能。三维电极电解法通过增大电极表面积实现低电流密度下电解,减小了浓差极化,从而提高了电流效率。目前使用三维电极电解处理废水中的Cu“已经取得了较好的效果,并已应用于实践中。R-C•Wjdener等人使用网状玻璃炭电极对酸性含铅废水进行了研究,在一O.8 V(vs.SCE)的电位下,使用O.5moL/L硼酸作缓冲溶液,得出最佳条件是阴极孔隙率80 ppi,流速240L/h。可使初始浓度为50mg/L的含铅废水降至0.1 mg/L,电流效率还可达到14%。实现了含铅废水的深度净化。
(四)化学沉淀法除砷原理:
水体中的砷如何去除:目前,国内外处理污水处理中含砷废水的方法主要有沉淀法、离子交换法、生物法、膜法、电凝聚法、吸附法等。这些方法均有其自身的特点,如:沉淀法除砷技术较为完善,应用较为广泛,但它处理后会产生大量废渣,造成二次污染,而且除砷效率低,难以满足饮用水水质要求;离子交换法适用于处理量不大、组成单一、回收价值高的废水,但其处理工艺复杂、成本高,难以实现工业化生产;生物法中微生物对周边环境的要求很严格,因砷具有毒性,用此法处理水中的砷目前尚处在起步阶段;膜分离法处理成本较高,不宜大规模应用;电凝聚法操作技术条件要求比较高;吸附法是利用吸附剂提供的大比表面积,通过砷污染物与吸附剂间较强的亲和力达到净化除砷的目的。吸附法由于简单易行、去除效果好、能回收废水中的砷、对环境不产生或很少产生二次污染,且吸附材料来源广泛、价格低廉、可重复使用等优势而备受人们关注。
石灰法除砷原理:
一般适用于含砷较高的酸性废水。投加石灰乳,使其与砷酸根或亚砷酸跟离子发生反应,生成难溶解的砷酸钙或亚砷酸钙沉淀。
化学原理:
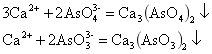
废水投加石灰乳混合沉淀,当石灰乳投加适当,反应进行的完全时,出水水质可到达污水综合排放标准(GB8978-88).
此方法的缺点是反应较慢,而且生成的砷酸钙与亚砷酸钙在水中的溶解性较大。
石灰-铁盐法除砷原理:
一般用于含砷量较低的,PH值接近中性或者弱碱性的废水处理,利用砷酸盐或亚砷酸盐能与铁、铝等金属离子形成稳定的络合物,
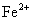 在鼓入空气的条件下转变成
在鼓入空气的条件下转变成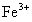 ,同时
,同时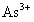 转变成毒性较小的
转变成毒性较小的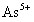 ,从而生成溶度积非常小(
,从而生成溶度积非常小(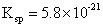 )的
)的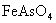 沉淀。另外
沉淀。另外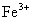 的水解产物
的水解产物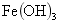 对一些难降解的细小的
对一些难降解的细小的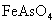 和
和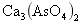 颗粒有吸附、凝聚、网捕的作用。
颗粒有吸附、凝聚、网捕的作用。硫酸亚铁铁离子除砷法是利用铁离子或其化合物对砷离子进行吸附共沉来达到除砷的目的。这种方法主硫酸亚铁除砷要针对砷的水体污染。这种方法除砷,对水体中的酸碱性要求比较高,一般是在5.5-8.5这个范围内,一般是对含砷污水添加硫酸亚铁等铁盐混凝剂进行酸碱调节(硫酸亚铁处理碱性废水),同时增加污水中铁的含量。水中的铁离子含量保持在或者高于1.5mg/l。所投加的铁离子与污水中的砷离子的比例不得少于20:1,就可以使其去除率达到80%-95%。
废水中砷主要以正亚砷酸和偏亚砷酸及它们的盐类的形式存在,废水中有下列电离平衡:
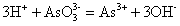
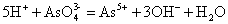
在废水中加入
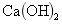 、
、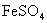 时,铁和废水中
时,铁和废水中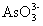 、
、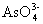 形成稳定的络合物,并被铁的氢氧化物吸附共沉而达到除砷的目的:
形成稳定的络合物,并被铁的氢氧化物吸附共沉而达到除砷的目的:
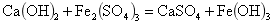
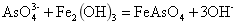
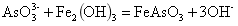
其中,
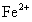 有很强的还原性,在溶液中很容易被氧化成
有很强的还原性,在溶液中很容易被氧化成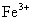 。
。硫化物法除砷原理:
在酸性条件下,砷以阳离子形式存在,当加入硫化剂时,生成难溶的
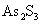 沉淀。硫化法净化效果较好,可使废水中含砷量将至0.05mg/L一下。废水PH值与转化法除砷的关系由废水砷化合物的性质决定的,砷酸和亚砷酸均为两性化合物,在水中既能按酸式电离,也能按碱式电离。酸性条件下,碱式电离将向生成砷离子方向移动。
沉淀。硫化法净化效果较好,可使废水中含砷量将至0.05mg/L一下。废水PH值与转化法除砷的关系由废水砷化合物的性质决定的,砷酸和亚砷酸均为两性化合物,在水中既能按酸式电离,也能按碱式电离。酸性条件下,碱式电离将向生成砷离子方向移动。主要化学反应式如下:
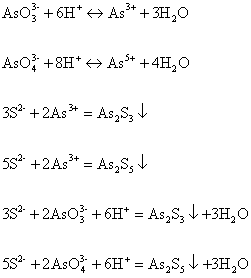
但硫化物沉淀需要在酸性条件下进行,否则沉淀物难以过滤,上清液中存在过剩的硫离子,在排放之前,需要进一步的处理。由于
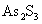 沉淀物只有在酸性环境中才能稳定,当PH值>1时,
沉淀物只有在酸性环境中才能稳定,当PH值>1时,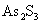 将会重新溶解到废酸溶液中,所以处理过程中,硫化物的加入量控制非常关键,硫化物投入量不足时,不能充分去除砷氧化物;投入量过多,又会过多消耗废酸溶液中的
将会重新溶解到废酸溶液中,所以处理过程中,硫化物的加入量控制非常关键,硫化物投入量不足时,不能充分去除砷氧化物;投入量过多,又会过多消耗废酸溶液中的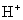 离子,使酸度过低,甚至呈碱性,造成
离子,使酸度过低,甚至呈碱性,造成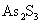 的重新溶解。这两种情况都会使除砷效率严重下降。
的重新溶解。这两种情况都会使除砷效率严重下降。